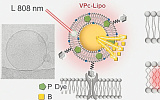
Нуклеосомы из четырех молекул гистонов, обвитые молекулами ДНК. Белые шарики – метильные группы –СН3; розовые – ферменты. Иллюстрация Physorg
Нуклеосомы из четырех молекул гистонов, обвитые молекулами ДНК. Белые шарики – метильные группы –СН3; розовые – ферменты. Иллюстрация Physorg
Знаменитый английский естествоиспытатель Уильям Гарвей, открывший два круга кровообращения, выпустил в 1651 году книгу, которая называлась «De Generatione Animalium» («О происхождении животных»). Так родилась концепция преформизма, которая постулирует присутствие уже сформировавшегося организма в головке мужского спермия. Идею поддержал голландский физик-оптик Николаас Хартсекер, будто бы увидевший с помощью линзы маленького ребенка – petit enfant – в спермии. Недаром Карл Бэр трактовал название спермиев как «семена животных».
Сегодня, начиная с 2008 года, эпигенетику определяют как наследование признаков (фенотипа) без изменений ДНК-последовательности букв (нуклеиновых кислот) генетического кода. Молекулярный механизм, ответственный за эпигенетические феномены, – метилирование, то есть присоединение к ДНК метильных групп –СН3. Это приводит к выключению активности, или «заглушению» (silencing) генов. Это один из клеточных механизмов регуляции генов наряду с РНК-интерференцией, за открытие которой вручили Нобелевскую премию в 2006 году. А в 2012 году ее присудили за генетическое репрограммирование клеток взрослого организма с получением стволовых клеток.
Десять лет назад была высказана идея, что эпигенетика «в лице» ДНК-метилирования может определять биологический возраст людей. Ее экспериментально, после обследования людей старше 56 лет, подтвердили в университете Южной Калифорнии в Лос-Анджелесе. Попутно было выяснено, что с возрастом ускоряется ДНК-метилирование, которое является надежным предсказателем жизненных исходов.
В парижской Сорбонне определили, что «старые» (senescent) клетки определяют опухолевую прогрессию у подопытных мышей с моделью мозговой опухоли (глиобластомы). Удаление «пожилых» клеток меняло опухолевую экосистему (ТМЕ – туморное микроокружение). Как результат – увеличение продолжительности жизни грызунов. Эта работа представлена в журнале Nature Communications.
В 2009 году журнал Science Advances представил статью генетиков из Института сердечных и легочных заболеваний в немецком Бад-Наухейме. Исследователи доказали, что мутации родителей влияют на активность генов у их потомков. А совсем недавно в Европейской лаборатории молекулярной биологии в Гейдельберге было показано, что метильные отпечатки отдельных молекул регулируют активность белковых транскрипционных факторов, активирующих транскрипцию-«переписывание» генов (Molecular Cell).
И все же окончательную ясность в решение запутанного биологического вопроса внесли ученые Университета Ла-Джолла. Там получили эпигенетическое наследование обжорства (obesity) у мышей на протяжении четырех поколений. Статья ученых в журнале Cell называется «Трансгенерационное наследование приобретенных эпигенетических сигнатур у мышей». Генерациями в данном случае названы поколения, а термин «сигнатура» можно перевести как признак, маркер или свойство. Речь в этом случае идет о получении метилированных по гену белкового рецептора «плохих» липидов низкой плотности, переносящих в крови жировые молекулы. «Замалчивание» рецепторного гена приводит к набору мышами излишнего веса.